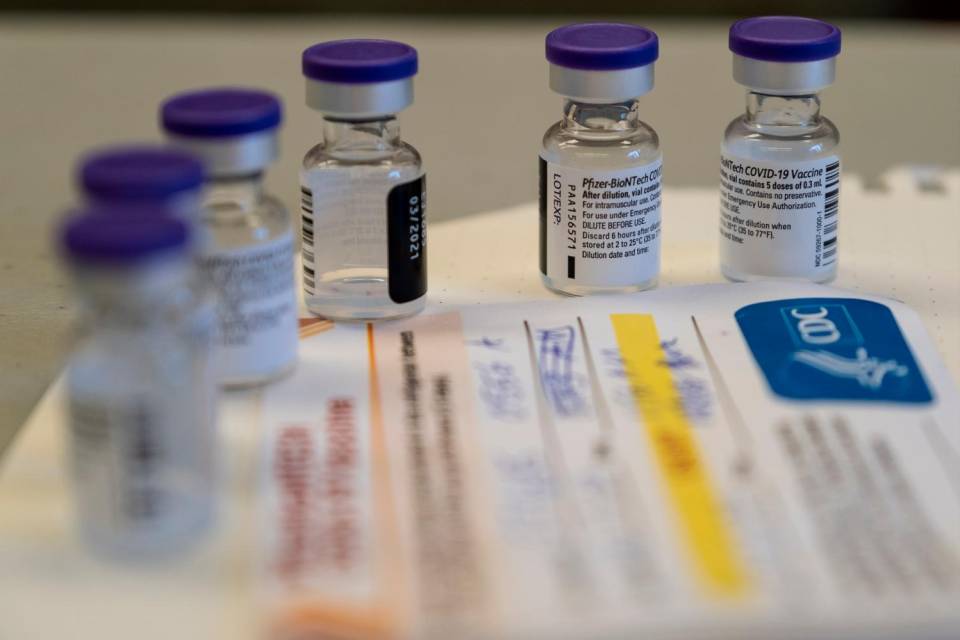
 L'Ema (Agenzia europa per i Medicinali), ha raccomandato oggi di concedere un'autorizzazione all'immissione in commercio condizionata per il vaccino anti Covid-19 Comirnaty, sviluppato da BioNTech e Pfizer, da somministrare alle persone a partire dai 16 anni di età.
L'Ema (Agenzia europa per i Medicinali), ha raccomandato oggi di concedere un'autorizzazione all'immissione in commercio condizionata per il vaccino anti Covid-19 Comirnaty, sviluppato da BioNTech e Pfizer, da somministrare alle persone a partire dai 16 anni di età.Il parere scientifico dell'Ema apre la strada alla prima autorizzazione all'immissione in commercio di un vaccino anti Covid-19 nell'Ue da parte della Commissione europea, con tutte le garanzie, i controlli e gli obblighi che ciò comporta. La Commissione si è impegnata a ridurre a due giorni, dopo la raccomandazione positiva dell'Ema, il tempo necessario a dare la sua autorizzazione finale, dopo aver consultato gli Stati membri.
"Il comitato per i medicinali per uso umano (Chmp) dell'Ema ha completato la sua rigorosa valutazione del vaccino Comirnaty, concludendo per consenso che sono ora disponibili dati sufficientemente solidi sulla qualità, sicurezza ed efficacia del vaccino da poter raccomandare un'autorizzazione formale all'immissione in commercio condizionale. Ciò fornirà un quadro controllato e solido per sostenere le campagne di vaccinazione a livello dell'Ue e proteggere i cittadini europei", si legge in un comunicato stampa dell'Ema.
 16° C
16° C LIVE
LIVE


IL COMMENTO
-
Luigi Leone
Lunedì 07 Aprile 2025
-
Mario Paternostro
Domenica 06 Aprile 2025
leggi tutti i commentiDai dazi di Trump al voto per Genova, quando il mondo va alla rovescia
"Ti ricordi Bilancia?" 17 vittime scelte per odio e per caso